Accompagné des ministres de la santé et de l’éducation, Emmanuel Macron a annoncé, mardi 28 février à Jarnac, en Charente, une campagne de vaccination « généralisée » dans les collèges pour éradiquer le papillomavirus. « On va généraliser (la vaccination) à partir de la rentrée prochaine pour les 5e », a indiqué le chef de l’Etat lors d’une rencontre avec des élèves dans un collège (…) « Cela permet d’éviter beaucoup de cancers », a ajouté Emmanuel Macron.
Le Monde 28 février 2023.
La France, parmi tous les pays dits « développés » est vraiment, dans ce domaine, à la traîne. Tous les professionnels concernés par la pathologie ou la prévention des infections dues aux Papillomavirus (HPV), réclamaient depuis longtemps un message fort en faveur de la vaccination universelle de l’adolescent qui a du mal à prendre son envol. On ne pourra donc pas se plaindre de cette déclaration. Le vrai problème est de savoir ce qu’il y aura derrière cette annonce.
Parallèlement à l’amélioration du dépistage, il y a, en effet, une impérieuse nécessité à améliorer la couverture (CV) mais aussi le rattrapage vaccinal de nos adolescents et jeunes adultes pour ne pas sacrifier une partie importante de chaque cohorte annuelle de naissance. Si des pays, comme l’Australie, la Grande-Bretagne ou le Portugal, montrent l’exemple et ont de bonnes couvertures vaccinales (CV), il existe une mauvaise situation générale qui n’est pas que française. La note de synthèse de l’OMS de décembre 2022 souligne un contexte très préoccupant de déclin post-Covid de la couverture vaccinale contre le HPV à l’échelle mondiale. Entre 2019 et 2021, la couverture par la première dose de vaccin contre le HPV est passée de 25 % à 15 %. Cela signifie qu’en 2021, dans le monde, 3,5 millions de filles de plus qu’en 2019 n’ont pas pu bénéficier de ce vaccin[1].
L’impact des infections HPV est pourtant bien établi (Bulletin du cancer, 2020[2]). S’il s’agit de la plus importante maladie sexuellement transmise dans le monde, elle ne se limite pas à ça. Il s’agit surtout d’une infection responsable de verrues génitales et de cancers essentiellement génitaux, anaux et oropharyngés. Si la transmission est essentiellement sexuelle, elle se fait globalement de peau à peau et par les muqueuses[3] . Par ailleurs, de l’ADN de l’HPV a pu être retrouvé plusieurs jours sur certaines surfaces, sous-vêtements, sondes vaginales[4], sans que la preuve de son caractère contaminant n’ait cependant pu être apportée[5].
L’importance des cancers viro-induits a été bien précisée par la Ligue contre le Cancer, dans le Livre blanc de la prévention des cancers en 2018[6]. En ce qui concerne les cancers « évitables », les infections sont en 5eme position avec, en tête, l’HPV, bien avant la pollution atmosphérique ou les radiations ionisantes. (fig1)
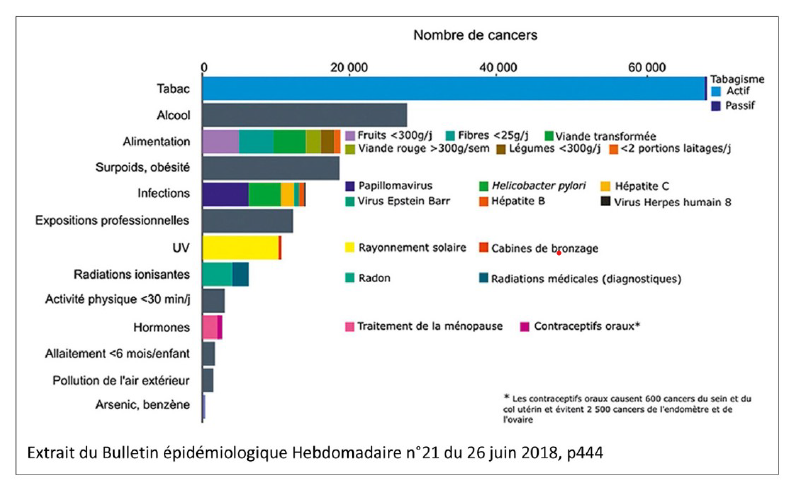
Tout le monde connait le poids de l’infection HPV dans la genèse de cancers. Sur plus de 6000 cancers HPV induits annuels, 2/3 surviennent chez la femme et 1/3 chez les hommes (fig2). Il n’y a quasiment pas de cancer du col sans HPV. Les cancers de l’anus sont dus à HPV dans 90% des cas[7]. Mais surtout, l’impact actuel de l’HPV dans les cancers oro-pharyngés ne fait que croître. Aux USA, ils deviennent maintenant plus fréquents que les cancers du col. Des données encore parcellaires, non publiées, sembleraient montrer la même évolution au moins dans la région parisienne.

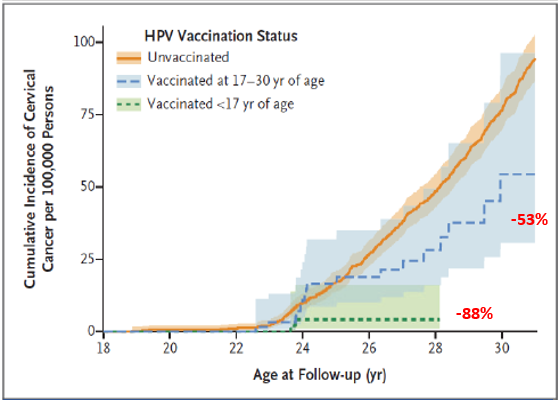
Les vaccins existent depuis 2007 et la preuve de leur efficacité n’est plus à apporter. En raison de l’histoire « naturelle » qui va de l’infection HPV au cancer sur une période de 10 à 30 ans, l’efficacité clinique n’a d’abord pu être évaluée que sur les lésions qui apparaissent les premières : les verrues génitales puis les lésions pré-cancéreuses du col de l’utérus. Mais, maintenant, nous avons les données sur les cancers eux même. Nous savons que cette efficacité est meilleure lorsque la vaccination est pratiquée avant l’âge de 17 ans (88% ; IC 66-100) [8] (Fig3). La durée de protection est tout à fait suffisante pour que la vaccination soit faite tôt, c’est-à-dire à 11 ans en même temps que la vaccination DTPC et sans, pour l’instant, nécessité de rappels ultérieurs.
S’il est préférable de la faire tôt, la vaccination reste toujours très intéressante après 17 ans (55% de réduction du risque de cancer du col, Fig3). Le critère « avant tout rapport sexuel » ne doit plus être un frein et doit être abandonné complètement.
De plus en plus de données vont aussi dans le sens d’un intérêt non négligeable chez les femmes adultes ayant déjà été prises en charge pour des lésions HPV induites.
Sur le plan de la tolérance, avec 16 ans de recul (sortie et recommandation des vaccins en 2007), toutes les craintes ont pu être démenties. L’OMS (GACVS) a fait son rapport sur le sujet en juillet 2017[9] avec 270 millions de doses injectées. Aucune augmentation de maladies graves par rapport à l’incidence attendue des mêmes maladies n’a pu être retrouvée. Par ailleurs, aucune étude n’a mis en évidence de lien avec une maladie auto-immune ou autre.
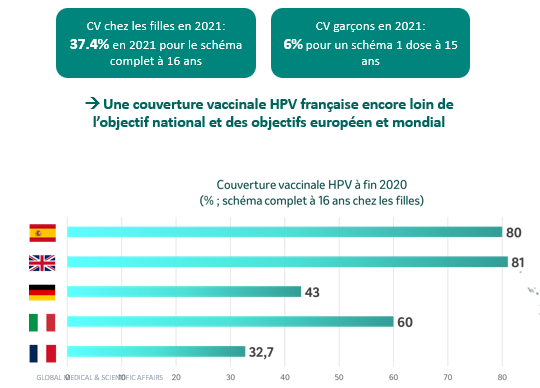
En France, la couverture vaccinale remonte depuis 2015 (Fig 4) mais elle reste très en-dessous des objectifs, en particulier par rapport à celle des pays socio-économiquement comparables (Fig 5) :
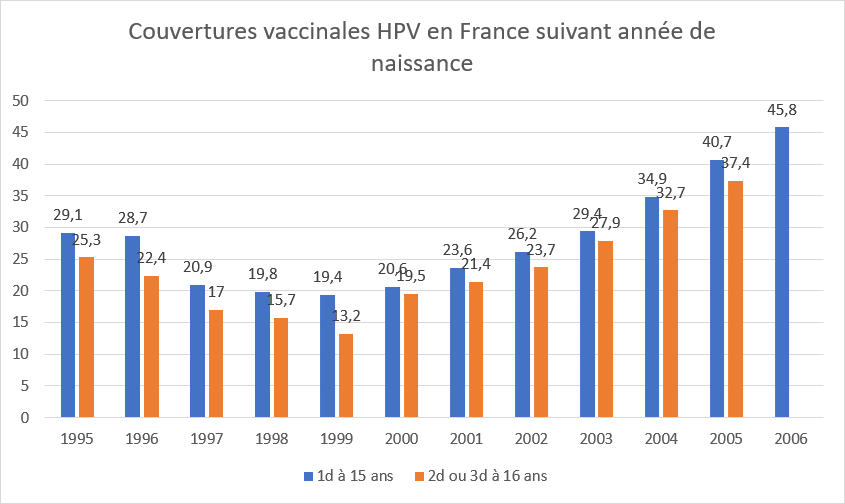
Pour les filles, l’OMS s’est donnée pour objectif une CV de 90% dans le monde et l’INCA, 80% en France[10]. Pour les garçons, l’introduction ne fait que commencer en France (2021). 12 mois après celle-ci, la CV ne dépasse pas 6% (Fig 5). A titre de comparaison en Suède où le vaccin a été introduit en 2020 pour les garçons, la CV est montée à 85%.
Que pourrions-nous faire ? Tout d’abord, comment fait-on à l’étranger ? En janvier 2023, 101 pays vaccinent à l’école. En 2017, 12 pays européens le faisaient déjà[11]. Ce sont ces pays qui ont la meilleure CV[12].
Schématiquement trois systèmes de vaccinations s’opposent : un premier système que nous pourrions qualifier « d’institutionnel » : centres de vaccination publics et milieu scolaire, un deuxième que nous appellerons « libéral » comme en France et un système mixte. La figure 6 montre le lien entre CV et systèmes. Si le système institutionnel a manifestement un avantage, un lien de causalité ne peut pas être affirmé péremptoirement. Des facteurs culturels, par exemple, peuvent s’y rajouter. L’expérience belge qui a deux communautés et un système mixte commun montre une nette différence entre Flamands et Wallons. En France Il existe d’ailleurs de grosses disparités d’une région à l’autre avec un système de santé commun : 35% ou plus dans le nord, moins de 20% en PACA. Imposer brutalement un système institutionnel à un pays « gaulois » n’est donc pas forcément gage de réussite…
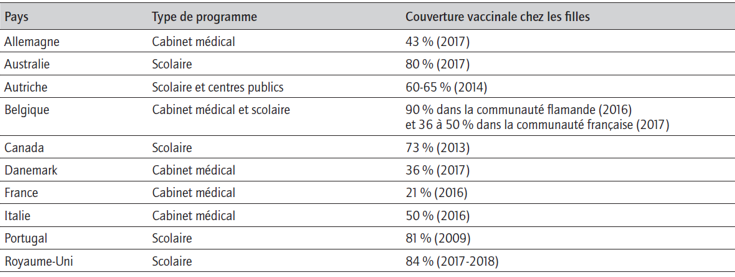
La revue de la littérature de S. Bruel parue en 2020 [13] et dont est tiré le tableau de la figure 6, conclut par ailleurs que les interventions éducatives seules augmentent la connaissance sur le HPV ainsi que l’intention vaccinale mais malheureusement pas la vaccination elle-même.
En France, la vaccination en milieu scolaire subit deux freins. D’une part, la médecine scolaire est exsangue. D’autre part, reste en mémoire la polémique du lien, pourtant récusé depuis des décennies, entre vaccination hépatite B et SEP, lorsque cette vaccination avait été introduite à l’entrée au collège dans les années 1990 (les ministres Douste Blazy puis Kouchner). Depuis le sujet était resté quasiment tabou.
La période Covid, espérons-le, a peut-être changé l’image de la vaccination en dispensaires, centres de santé ou, pourquoi pas, au collège.
Une première expérimentation de vaccination en collège (en 5ème, projet PrévHPV) a été réalisée dans le Grand Est (Meuse et Vosges) pendant deux ans et son analyse publiée en juin 2022. Elle a montré d’assez bons résultats chez les jeunes scolarisés en classe de 5e mais qui sont restés modestes. Le taux de vaccination est passé de 9 % à 27 % la première année et de 14 % à 31 % la seconde.[14] En moyenne, 20% (8% à 32% selon le collège) des parents ont consenti à la vaccination de leurs enfants en collège, et 16% (8% à 26%) des élèves ont pu être effectivement vaccinés (écart entre consentements et vaccinations principalement lié à l’absence de carnet de vaccination de l’élève le jour de la vaccination, vaccination par le médecin traitant…[15] D’autres facteurs peuvent être intervenus puisque cette augmentation de la CV est retrouvée au niveau national (cf Fig 4).
Plus que l’amélioration de la CV immédiate, l’intérêt de cette action est d’avoir initié des actions de formation, d’information et de motivation à l’intérieur des collèges (élèves, enseignants) et hors des établissements (parents et professionnels de santé). Elles devraient avoir un impact à plus long terme. La médecine scolaire n’a pas été vraiment impliquée.
Quelles actions semblent apporter leurs fruits au niveau international ? Une revue de la littérature internationale portant sur la période 2012-2022 a été présentée à Bilbao en février 2023 (Eurogyn 2023[16]). La conclusion porte sur le caractère favorisant d’un certain nombre de démarches jugées positives :
- Les campagnes de sensibilisation des parents et des élèves
- La formation des professionnels de l’éducation et de la santé scolaire
- Des systèmes d’invitation et de rappels (relances)
- Le système de refus écrit (opt-out) plutôt que celui de « opt-in » (consentement écrit). Dans le cas où ce dernier est choisi, il faut qu’il soit court, simple et accompagné de messages éducatifs
- Un front uni avec des messages communs pour faire face à une éventuelle défiance et à la désinformation sur le sujet.
Cependant la réussite d’un programme dépend aussi du contexte, de l’existence d’une somme d’actions confluentes, ainsi que d’un consensus social et médical. C’est peut-être là que se pose le problème en France. Notre système libéral a de multiples avantages. Il existe un lien patient – médecin fort, permettant confiance et consentement éclairé.
Même si l’accès aux soins primaires s’est dégradé en France, il reste meilleur que dans les pays où la santé se fait en dispensaire.
Les points négatifs sont cependant nombreux :
- Parcours de vaccination compliqué qui nécessite une prescription médicale puis un achat en pharmacie et enfin un retour vers le médecin prescripteur pour injection. Deux mesures permettraient de résoudre ce problème. Une première semble à l’ordre du jour, c’est l’extension des compétences des pharmaciens et des infirmiers. Une autre mesure, dont on parle depuis longtemps mais qui ne semble pas avoir l’aval des autorités, serait de mettre à disposition des vaccins dans les cabinets médicaux.
- Hésitation vaccinale « record » : les campagnes de communication médiatiques et médicales, de formation des professionnels de santé, d’intervention de sensibilisation dans les collèges permettraient de lutter contre celle-ci. Les messages forts des autorités de santé y ont déjà contribué : loi sur les obligations vaccinales de 2018 qui a amélioré l’image vaccinale, y compris pour les adolescents non concernés par cette loi et récemment le message d’E. Macron.
- Non vaccination dans les lieux même où vivent les sujets concernés : collèges pour la vaccination HPV par exemple.
Un certain nombre d’interrogations vont devoir être précisées :
- Qui pourra vacciner en milieu scolaire ? La médecine scolaire disparaissant malheureusement progressivement, ce n’est pas elle qui pourra l’assurer, en tout cas pas tant qu’un plan de sauvetage de celle-ci ne sera pas décidé et appliqué. Comme dans le Grand Est, cela se fera-t-il sur un mode « Covid » : appels à volontaires, déplacement des centres de santé… ??
- Qui doit on vacciner ? Certes la vaccination avant 17 ans doit être privilégiée et la classe de 5ème parait une bonne cible mais le rattrapage universel au moins jusqu’à 26 ans doit aussi être rendu possible alors qu’il est encore limité à 19 ans.
- Quelle prise en charge ? Le reste à charge pour les patients ayant une mutuelle, ou en CMU est en principe déjà nul. L’accès pourrait être cependant facilité pour une petite partie de la population en situation de précarité.
- Obligation ? Quoiqu’il en soit une obligation vaccinale n’aurait qu’un effet d’annonce car elle semble difficilement applicable chez l’adolescent, chez qui il sera difficile de trouver une sanction ou une récompense à appliquer.
Au total, la vaccination HPV représente un réel challenge de santé publique pour les autorités, les professionnels de santé mais aussi les adolescents et leurs parents eux même. Échouer équivaudrait à une non-assistance à personne en danger. 1500 adultes plus ou moins jeunes meurent encore tous les ans en France de cancers HPV induits, malgré un dépistage systématique, une vaccination efficace, sûre et remboursée.
En conclusion
Parmi les actions qui permettrait d’accélérer la couverture vaccinale, de nombreuses pistes pourraient être tentées comme l’extension des compétences vaccinales des pharmaciens et des infirmières, la possibilité de rattrapage jusqu’à 26 ans quel que soit le sexe et les orientations sexuelles, les campagnes d’information massives en particulier en faveur des populations défavorisées. La vaccination en milieu scolaire en est certainement un élément indispensable quoique probablement insuffisant.
Références
- L’OMS actualise ses recommandations concernant le calendrier de vaccination contre le PVH (who.int)
- Vié le Sage F, Cohen R. Prévenir les cancers : place de la vaccination Papillomavirus en population générale [Preventing cancer: The role of Papillomavirus vaccination in the general population]. Bull Cancer. 2020 Jan;107(1):10-20. French. doi: 10.1016/j.bulcan.2019.12.006. Epub 2020 Jan 22. PMID: 31982092.
- Gavillon N, Vervaet H, Derniaux E, Terrosi P, Graesslin O, Quereux C. Papillomavirus humain (HPV) : comment ai-je attrapé ça ? [How did I contract human Papillomavirus (HPV)?]. Gynecol Obstet Fertil. 2010 Mar;38(3):199-204. French. doi: 10.1016/j.gyobfe.2010.01.003. Epub 2010 Feb 26. PMID: 20189438.
- M’Zali F, Bounizra C, Leroy S, Mekki Y, Quentin-Noury C, et al. (2014) Persistence of Microbial Contamination on Transvaginal Ultrasound Probes despite Low-Level Disinfection Procedure. PLoS ONE 9(4): e93368. doi:10.1371/journal.pone.0093368
- Eric J Ryndock & Craig Meyers (2014) A risk for non-sexual transmission of human papillomavirus?, Expert Review of Anti-infective Therapy, 12:10, 1165-1170, DOI:10.1586/14787210.2014.959497
- https://www.ligue-cancer.net/article/47726_decouvrez-le-livre-blanc-des-premiers-etats-generaux-de-la-prevention-des-cancers
- Human papillomavirus genotype distribution in anal cancer in France: The EDiTH V study. Abramowitz L, Jacquard AC, Jaroud F, Haesebaert J, Siproudhis L, Pradat P, Aynaud O, Leomach Y, Soubeyrand B, Dachez R, Riethmuller D, Mougin C, Pretet JL, Denis F. Int J Cancer 2011; (129) 433-439.
- Lei J, Ploner A, Elfström KM, Wang J, Roth A, Fang F, Sundström K, Dillner J, Sparén P. HPV Vaccination and the Risk of Invasive Cervical Cancer. N Engl J Med. 2020 Oct 1;383(14):1340-1348. doi: 10.1056/NEJMoa1917338. PMID: 32997908.
- Relevé épidémiologique hebdomadaire, 14 juillet 2017, vol. 92, 28 (pp. 393-404) https://www.who.int/wer/2017/wer9228/fr/
- INCa 2021. Stratégie décennale de lutte contre les cancers 2021-2030- Feuille de route 2021-2025. Février 2021
- Nguyen-Huu NH, Thilly N, Derrough T, Sdona E, Claudot F, Pulcini C, Agrinier N; HPV Policy working group. Human papillomavirus vaccination coverage, policies, and practical implementation across Europe. Vaccine. 2020 Feb 5;38(6):1315-1331. doi: 10.1016/j.vaccine.2019.11.081. Epub 2019 Dec 10. PMID: 31836255.
- Perman S, Turner S, Ramsay AI, Baim-Lance A, Utley M, Fulop NJ. School-based vaccination programmes: a systematic review of the evidence on organisation and delivery in high income countries. BMC Public Health. 2017 Mar 14;17(1):252. doi: 10.1186/s12889-017-4168-0. PMID: 28288597; PMCID: PMC5348876.
- BRUEL Sébastien, COCHARD Julie, ESPINOUSE Sandrine et al., « Revue de la littérature sur les interventions en milieu scolaire concernant la vaccination anti-HPV », Santé Publique, 2020/1 (Vol. 32), p. 29-41. DOI : 10.3917/spub.201.0029. URL : https://www.cairn.info/revue-sante-publique-2020-1-page-29.htm
- Prévention cancer -Papillomavirus : vaccination généralisée à la rentrée 2023 pour les élèves de 5e | Service-public.fr et http://www.planetepublique.fr/
- CP 6 mars 2023 : « Vers l’acceptabilité de la vaccination contre les papillomavirus humains en France avec le projet PrevHPV » www.univ-lorraine.fr
- Marisa Felsher, Meheret Shumet, Cristinela Velicu, Ya-Ting Chen Human Papillomavirus Vaccination Delivery Systems Within National and Regional Immunization Programs: A Systematic Literature Review; Eurogyn 2023